암 치료 필수 세포 자가포식 신호 전달 경로 규명
백성희 서울대 생명공학과 교수 연구팀은 지금까지 잘 알려져 있지 않은 오토파지의 작동 기전을 세포 내 새로운 신호의 발견을 통해 규명했다고 16일 밝혔다.
오토파지는 세포에서 영양분 결핍, 대사성 스트레스, 감염, 노화, 암, 퇴행성 뇌질환 발병 등의 신호에 대해 활성화 되는 필수적 기작이다.
그동안 오토파지에 대한 연구는 세포질에서 오토파지 단백질들이 어떻게 결합하고 기능하는지에 대해서만 연구초점이 맞춰져 오토파지의 작동원리에 대해서는 전무한 상황이었다.
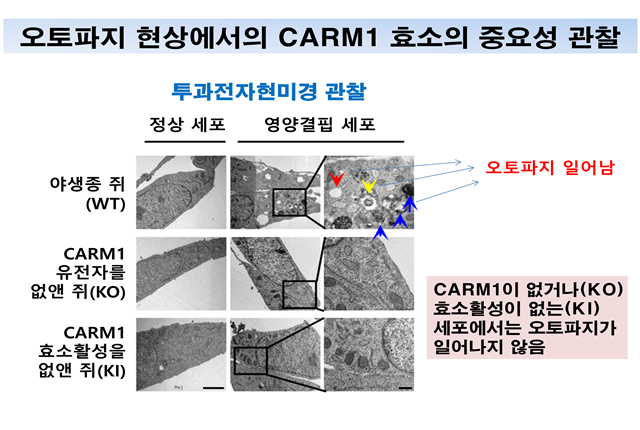
CARM1 효소가 세포 내에서 안정적인 상태를 유지하면 유전자가 발현돼 오토파지 현상이 활성화되지만, CARM1 효소가 분해돼 버리는 경우에는 오토파지 현상이 일어나지 않는다는 것이다.
연구팀에 따르면 세포에 당 결핍 상황을 유도했을 때 CARM1이 증가돼 오토파지 현상이 증가하고 반대로 세포내 영양소가 풍부한 상황이라면 'SKP2'라는 단백질이 CARM1을 분해해 오토파지 현상을 억제한다.
아울러 연구팀은 쥐를 이용한 실험을 통해 CARM1 효소를 억제하는 '엘라그산(Ellagic acid)'이라는 물질을 발견했다.
연구팀은 실험에서 쥐를 굶기고 간 조직을 관찰, CARM1 효소가 증가돼 오토파지 현상이 활성화된 간 조직에 엘라그산을 처리하면 CARM1 효소활동이 억제돼 오토파지가 억제되는 것을 확인했다. 엘라그산은 베리류에서 많이 검출되는 화학물질로 말라리아 치료제로 사용되고 있다.
백성희 교수는 "체내 항상성을 유지하는 오토파지 기능이 제대로 작동하지 않을 경우 암, 퇴행성 뇌질환 등의 병이 발생할 수 있다"며 "이에 따라 이번 연구에서 발굴한 오토파지 조절에 필수적인 신호전달 경로를 표적으로 하는 신개념 치료제 개발이 가능할 것으로 기대한다"고 말했다.
이번 연구결과는 국제 학술지 '네이처(Nature)'에 지난 15일자로 게재됐다.
댓글 정렬