김용성 아주대 교수 '세포침투 간섭항체' 원천기술 개발
오름테라퓨틱 창업으로 글로벌 시장 경쟁력 기대
김용성 아주대학교 교수 연구팀은 세포 내부 종양유발 라스(Ras) 돌연변이 단백질을 직접 표적해서 종양성장을 막는 치료용 항체기술을 개발했다고 22일 밝혔다.
라스 돌연변이 단백질은 가장 널리 알려진 종양유발 인자로 모든 인간 종양의 약 30%에서 발견된다. 특히 췌장암의 약 95%, 대장암의 약 52%, 비소세포폐암의 약 30%에서 확인돼 항체 개발이 매우 시급한 표적이다. 하지만 1982년 발견된 이후 30여년간 라스 돌연변이 단백질을 직접 표적하는 약물이 개발된 적이 없어 난공불락 표적으로 알려져 왔다.
기존 치료용 항체는 세포외부의 막단백질과 분비단백질만을 표적으로 암, 면역질환 등 다양한 질환 치료제로 개발돼 왔다. 하지만 세포질 내에 질환유발 단백질을 직접적으로 표적할 수 없는 한계가 있다.
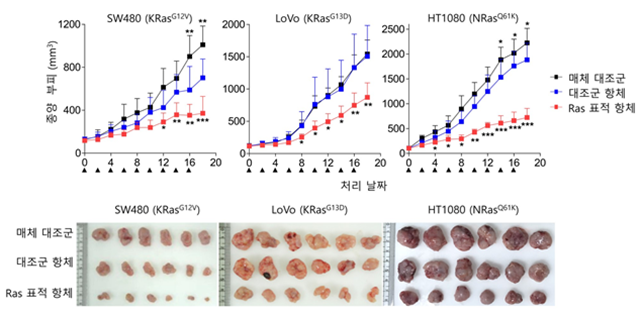
연구팀은 라스 돌연변이 단백질을 표적하면서 세포질 침투능이 있는 '세포침투 간섭항체' 원천기술을 개발, 종양세포의 성장과 분열, 촉진을 방해하는데 성공했다. 실험 쥐 모델을 통해 라스 돌연변이를 지닌 대장암과 섬유육종의 성장을 억제하는 결과를 확인했다.
이번 성과로 기존 항체가 표적하지 못했던 세포질 내의 많은 질환 관련 단백질을 항체로 직접 표적하는 플랫폼 기술을 제공 할 수 있을 전망이다. 연구팀은 2건의 국내특허와 미국, 유럽 등 14개국에 국외특허를 출원했다.
김용성 교수는 '세포침투 간섭항체' 원천기술 사업화를 위해 2016년 8월 이승주 박사와 오름 테라퓨틱를 공동창업했다.
김용성 교수는 "이번 연구성과는 항체가 종양세포에 침투해 라스 표적에만 선택적으로 결합하고 비정상적 신호 전달을 차단한 것"이라면서 "현재까지 없었던 라스 돌연변이 단백질을 직접 표적하는 신약 항체 치료제 개발 가능성을 열었다"고 의미를 강조했다.
이승주 대표는 "이번에 개발된 기술이 향후에 임상시험 단계를 거쳐 제품화로 이어지게 되면 2016년 기준 연간 900억 달러로 예측되는 국·내외 치료용 항체 시장에 진출할 수 있을 것"이라고 기대했다.
이번 연구는 미래창조과학부의 미래유망융합기술파이오니어 사업의 지원으로 이뤄졌다. 연구결과는 '네이처 커뮤니케이션즈 (Nature Communications)' 온라인 판 최신호에 10일 게재됐다.
댓글 정렬