미토콘드리아 내 펩타이드 자기조립 유도···'암세포 자살'
유자형 UNIST 교수 "난치성 암 치료법 기대"
UNIST(울산과학기술원·총장 정무영)는 유자형 자연과학부 화학과 교수팀과 곽상규 에너지 및 화학공학부 교수팀, 이은지 충남대 분석과학기술대학원 교수팀이 공동으로 암세포 미토콘드리아 내 합성 펩타이드 자기조립을 통해 암세포를 제거하는 새로운 항암 치료법을 개발했다고 22일 밝혔다.
기존 암 치료는 수술을 통해 암 조직을 제거한 뒤 화학 약물을 투여하는 방식으로 진행됐다. 화학 약물을 계속 투여하다 보면 내성이 생기며 더이상 화학 약물로 암을 억제하기 어렵다.
공동 연구팀은 이런 단점을 극복하기 위해 '분자의 자기조립(self-assembly)'을 이용해 암세포를 제거하는 새로운 치료법을 개발했다. 암세포 내부에서 스스로 뭉친 분자들이 암세포를 파괴하도록 만드는 방식이다.
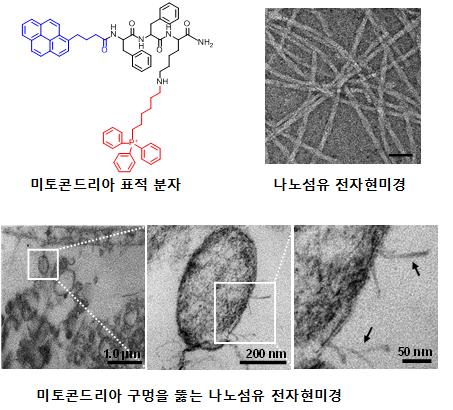
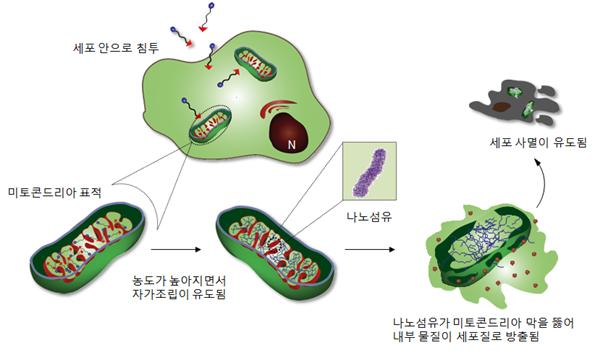
트리페닐포스포늄 펩타이드는 세포 밖에서 자기조립하지 못하고 분자로 존재한다. 하지만 이 분자가 미토콘드리아 안으로 들어가 쌓이면 그 농도가 수천 배 높아지게 된다. 이때 분자들끼리 끌어당기는 힘이 생기면서 자기조립해 나노섬유구조를 만들게 된다.
분자 하나가 암세포의 미토콘드리아에 끼치는 영향은 적다. 하지만 분자 수백~수천 개가 모여 만든 나노섬유구조의 영향력은 매우 커서 미토콘드리아 막에 구멍을 뚫게 된다. 미토콘드리아 안에 있던 단백질들이 세포질로 나오면서 암세포가 사멸하게 된다.
유자형 교수는 "이번에 개발한 방법은 화학 약물 치료와는 완전히 다른 메커니즘으로 암세포를 제거할 수 있기 때문에 약물 내성을 이겨낼 수 있다"라며 "난치성 암 치료법의 개발로 이어질 것으로 기대한다"고 말했다.
이번 연구성과는 '네이처 커뮤니케이션스(Nature Communications)'에 21일자 온라인판으로 발표됐다.
댓글 정렬