김진수 IBS 연구단·김대식 서울대 박사팀, 절단 유전체 시퀀싱 기법 활용해 규명
IBS(기초과학연구원·원장 김두철)는 유전체 교정 연구단(단장 김진수)과 김대식 서울대 화학부 연수연구원 박사팀이 유전자가위 처리 전과 후를 비교하는 프로그램을 활용, 염기교정 유전자가위가 기존에 사용되던 크리스퍼 유전자가위보다 정확성이 높다는 것을 규명했다고 11일 밝혔다.
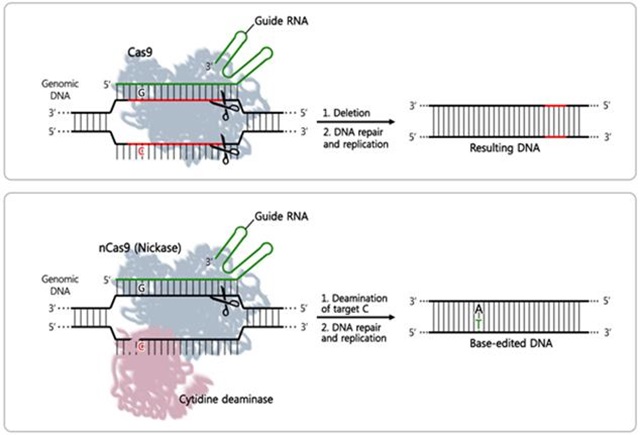
염기교정 유전자가위는 지난해 데이비드 리우(David R. Liu) 하버드 대학 연구 그룹과 케이지 니시다(Keiji Nishida) 고베 대학교 교수팀이 각각 개발해 세포 수준에서 적용한 바 있다. 이는 단일 염기를 교체할 수 있어 선천적 유전질환의 발병기전을 밝히고 치료법을 개발하는데 큰 도움이 될 것으로 기대됐다.
하지만 염기교정 유전자가위가 표적 위치에서 정확하게 작동하는지, 비표적 위치에서 오작동하지 않는지 거의 알려진 바가 없었다. 때문에 유전자 교정기법으로 널리 활용되기 위해서는 정확성에 대한 연구가 필요한 상황이었다.
연구팀은 2015년에 자체 개발한 절단 유전체 시퀀싱 기법(Digenome-seq)을 변형해 염기교정 유전자가위의 정확성을 유전체 전체 수준에서 규명했다.
절단 유전체 시퀀싱 기법은 유전자가위 처리 전과 후를 DNA의 서열을 분석하는 유전체 시퀀싱(Genome Sequencing)방법으로 비교해 잘린 위치를 구별하는 방식이다. IBS 연구진은 지난해 신형 유전자가위 크리스퍼 Cpf1의 정확성을 처음으로 밝히는데도 이 기법을 활용했다.
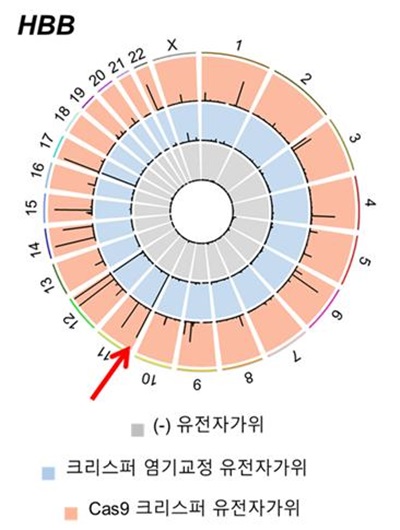
실험 결과, 크리스퍼 유전자가위는 평균 인간 유전체 32억 개 중 90곳을 자르는데 비해 염기교정 유전자가위는 평균 18곳에만 변이를 일으키는 것으로 나타났다. 이는 염기교정 유전자가위가 크리스퍼 유전자가위에 비해 비표적 위치에서 오작동할 확률이 현저히 낮아 정확성이 높다는 의미다.
또 연구진은 정확성이 더 높은 염기교정 유전자가위를 만드는 방법으로 교정할 DNA를 찾아가는 가이드 RNA 말단에 구아닌 염기를 추가해 길이를 조절하면 표적위치에서는 잘 작동하고 오작동할 확률을 줄일 수 있음을 확인했다.
이번 성과로 단일 염기 변이를 유도하거나 교정해야 하는 유전자와 줄기세포 치료제 개발, 고부가가치 농축산물 품종 개량 등에 널리 활용될 것으로 기대된다.
이번 연구결과는 생명공학 분야 학술지 '네이처 바이오테크놀로지' 11일 새벽 12시(한국시간)에 게재, 표지논문으로 선정 됐다. 연구진은 이에 앞서 지난 2월 28일 염기교정 유전자가위로 동물의 특정 유전자 염기를 바꾸는데 최초로 성공해 같은 학술지에 연구성과를 게재한 바 있다.
연구팀은 "염기교정 유전자가위가 크리스퍼 유전자 가위 기술만큼 널리 활용 될 수 있도록 더 정교하게 원하는 변이를 도입할 수 있는 기술로 발전시키기 위해 기여하고 싶다"고 말했다.
댓글 정렬