서울대·POSTECH 참여 공동연구팀, FKBP8 단백질 칼슘 수송
알츠하이머병·파킨슨병 등 치료제 개발에 새로운 표적 활용 기대

세포 내에는 다양한 세포 소기관들이 존재하며 제각기 역할을 하고 막으로 된 접촉부위를 통해 서로 소통한다. 특히 미토콘드리아와 소포체를 연결하는 MAM에 위치한 단백질들은 세포내 지질대사, 자가포식 등 핵심 기능을 조절한다.
미토콘드리아는 세포 내 에너지를 APT 형태로 공급하고 소포체는 단백질을 만들어서 세포 곳곳에 전달하는 세포소기관으로 서로 만나면 MAM이 형성되면서 칼슘의 이동통로가 된다. 이때 미토콘드리아로 칼슘이 과도하게 들어가면 미토콘드리아의 기능이 저하되면서 질환이 발생하게 된다. 때문에 최근 MAM이 세포내 신호전달이 오가는 허브로 주목받고 있다. 실제 신경퇴행성질환 환자들의 유전자 변성이 해당 부위에서 발견되기도 했다.
연구팀은 MAM에 위치한 단백질을 표지하고 분석하는 새로운 기법을 고안했다. 기존에는 단백질 구조를 분석하기 위해 원심분리법을 이용했는데 이는 분리과정 중 노이즈가 생기고 효율이 떨어지는 한계가 있어 연구팀이 이를 보완했다.
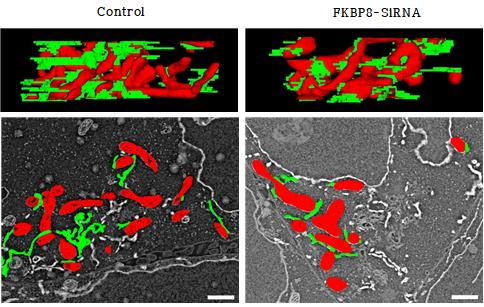
그 결과 살아있는 인간 세포에서 MAM을 구성하는 115개 단백질을 발견했다. 또 대면적 3차원 전자현미경을 이용해 MAM 부위를 3차원으로 관찰, 집중해 연구하던 FKBP8 단백질이 미토콘드리아와 소포체의 연결구조(MAM)를 변화시키면서 칼슘 수송에 필수적으로 기능한다는 사실을 밝혀냈다.
이번 연구는 신경퇴행성질환의 공통 원인으로 알려진 미토콘드리아의 칼슘 증가현상을 조절할 수 있는 단백질을 발견했다는데 의의가 있다. 향후 알츠하이머병, 파킨슨병 등의 치료제 개발에 새로운 표적으로 활용할 수 있을 것으로 기대된다.
공동 교신저자로 참여한 뇌연구원의 문지영 박사와 공동저자로 참여한 정민교 박사는 "세포소기관 사이의 네트워크가 제대로 이루어지지 않으면 질환이 발생하는데, 이에 관여하는 MAM 단백질을 보다 정확하게 동정해낸 것"이라며 "앞으로 미토콘드리아의 손상을 지연하거나 막을 수 있는 핵심 인자로서의 기능을 후속 연구할 예정"이라고 말했다.
댓글 정렬